概述
肥厚型心肌病(hypertrophic cardiomyopathy,HCM)是一种遗传性疾病,其特征为心室肥厚,心腔无扩大。HCM又称特发性主动脉瓣下狭窄(idiopathic subaortic stenosis,ISS)和不对称性室间隔肥厚(Asym-metric septal hypertrophy,ASH)。临床表现多样化,是较大儿童及青少年猝死原因之一。 小儿肥厚型心肌病包括一组不同病因的疾病,其特征是具有异常的不能解释的心室肥厚而心腔不扩大,以左心受累为主,右室心肌亦可受累,心室肥厚不对称、不均匀,心室腔变小,以左室血液充盈受阻、左室舒张期顺应性下降为基本病态,组织学上...[详细]
病因
目前已证实HCM是一种常染色体显性遗传病。先证者的同胞50%受累。大约50% HCM是由7个编码收缩蛋白基因突变引起,其中肌球蛋白重链基因突变占30%~40%。虽然相同基因突变所致的HCM亲属间常有显著不同的临床表现,但有几项研究表明HCM的表型主要由遗传缺陷所决定,如特定的形态学改变及猝死的发生等均与某种基因突变有关。
发病机制
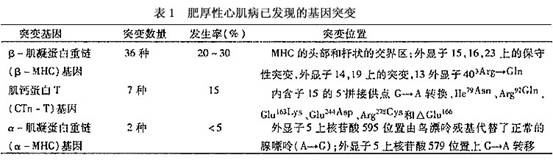
根据病因可分为原发性和继发性两大类,但近年来由于在代谢、遗传和分子水平研究取得重大进展,两者的分界已模糊不清。 1.原发性肥厚型心肌病 原发性HCM可呈家族性发病,也可有散发性发病,根据流行病学调查结果,散发者占2/3,有家族史者占1/3。家族性发病的患者中,50%的HCM病因不明确,50%的家系中发现有基因突变。遗传方式以常染色体显性遗传最为常见,约占76%。 (1)遗传因素:HCM具有遗传异质性,许多基因、多种突变都参与了HCM的发病(表1)。Jarcho应用基因连锁分析技术首次在家族性HCM患者中发现14号染色体q1长臂上的心脏β-肌凝蛋白重链(β-MHC)基因的错...[详细]
临床表现
儿童HCM多无明显症状,常因心脏杂音或家族中有HCM患者而首次就诊。临床表现具有多变性,并因发病年龄而不同。1岁以下婴儿较1岁以上儿童严重。60%婴儿HCM有左、右室流出道梗阻,常发生心力衰竭,多于1岁之内死亡。1岁以上儿童通常无症状,只有少数发生左室流出道梗阻,但较婴儿易发生猝死。婴儿常见症状有呼吸困难、心动过速、喂养困难,较重者发生心力衰竭,伴随青紫。心脏扩大,有心脏杂音或心律失常。少数儿童有呼吸加快、乏力、心悸、心绞痛、头晕、晕厥前兆及晕厥,并可于活动后发生猝死。即便无明显症状,也有发生猝死的危险。心力衰竭罕见。体征有脉搏短促、心尖搏动呈抬举样或双重性搏动。第1心音正常,第2心音多数正常...[详细]
并发症
常并发心力衰竭、心律失常,易发生猝死。
实验室检查
1.一般血液检查 主要是筛查可引起心肌肥厚的代谢性疾病,如检查空腹血糖、血中肉碱、乳酸盐、丙酮酸、氨基酸浓度等;检查尿中氨基酸、有机酸等成分及其含量。 2.心内膜心肌活检 考虑手术治疗时应做心导管检查和心血管造影,测定血流动力学参数、压力阶差、心室肥厚部位及程度、心腔变形、流出道狭窄及瓣膜反流等情况,少数婴儿HCM需做心肌活检,以除外Pompe病(Ⅱ型糖原贮积病),但后者骨骼肌活检可确定,而且安全。 肥厚心肌纤维排列紊乱,心肌细胞异常巨大,核周常有“光环”围绕,线粒体增生变性。组织化学测定有严重糖原堆积,免疫化学测定显示肥厚心肌内儿茶酚胺含量增高,具有诊断意义。 ...[详细]
其他辅助检查
1.心电图检查 可显示左室肥厚、ST段下降、T波倒置、左房肥大、异常Q波、QT间期延长。少数出现预激综合征或其他室内传导阻滞图形。婴儿患者常有右室肥厚,可能反映右室流出道梗阻。动态心电图监测可见室性期前收缩,室性及室上性心动过速,窦性心动过缓及房室传导阻滞。少数患儿心电图正常,但大多数患儿心电图明显异常: (1)左心室肥大。 (2)异常Q波(30%~50%):深、窄而持久不变,多见于Ⅰ,Ⅱ,Ⅲ,aVF,aVL或V4,V5导联。病理性Q波的形成,一方面与肥厚室间隔除极的初始向量向前上方运行有关,造成Ⅱ,Ⅲ,avF为异常Q波,右胸导联为高窄R波;另一方面与心肌纤维化、变性及排...[详细]
诊断
根据病史、家族史、临床表现及超声心动图检查,一般可以确诊。 1.梗阻型HCM 诊断HCM必须首先排除其他原因引起的心肌肥厚,如先心病、高血压、内分泌代谢病等。若存在胸痛、晕厥、心悸等症状,心脏检查发现心前区中晚期喷射性杂音,且杂音强度随体位、屏气、握拳等动作的改变而改变,心电图显示左心室肥厚、ST-T改变和异常Q波时,要考虑梗阻型HCM的诊断。若符合下列条件:心导管示左室流出道收缩期压差>2.67kPa(20mmHg),或虽<2.67kPa(20mmHg),但用药物负荷后压差增加;心血管造影示左室流出道狭窄;超声心动图示SAM现象,室间隔厚度/左心室后壁厚度之比为1.3~1.5,可...[详细]
治疗
1.药物治疗 应限制患者参加紧张或剧烈活动,避免运动后发生猝死。洋地黄、异丙肾上腺素、多巴胺等正性肌力药及强效利尿药应避免应用。正性肌力药可增加左室压力阶差,使临床症状加重,并可引发室性心律失常。强效利尿药减轻心室前负荷,致左室流出道梗阻加重。HCM收缩功能正常,因舒张功能障碍引起肺淤血,用利尿药应谨慎,并与普萘洛尔(心得安)合用。 有症状的HCM采用β阻滞药或钙阻滞药治疗。对无症状的患者是否应用尚有不同意见,但有明确的猝死家族史或严重心室肥厚的患者,则需用药。 (1)β阻滞药:通常用普萘洛尔(心得安)或阿替洛尔(氨酰心安),具有抗交感神经作用,可减慢心率,降低左室收缩力...[详细]
预后
小儿HCM临床表现多样化,预后不一。婴儿患者多于1岁内死亡,心力衰竭为主要死亡原因。曾报道1岁以上儿童HCM 37例,包括18例无症状者,随访1~12年(平均9年),死亡18例,年死亡率4.8%,高于成人的2%~3%。死亡原因:猝死11例(30%),心力衰竭 2例(5%),心肌切除术后3例(8%),感染性心内膜炎及自杀各1例。上述病例为选择性住院的高危患者,病死率高,不能代表总体情况。一般认为正确估计病死率约为1%或更低。 猝死常发生在年龄15~35岁,青少年及年轻成人HCM患者。猝死前大多无症状或仅有轻微症状,多于运动后发生。猝死高危的临床指征有: 1.晕厥或心脏停...[详细]
预防
重视做好遗传学咨询工作,其他措施有待病因学研究的进一步成果而定。

 HCM患儿心肌肥厚程度、肥厚的分布、发病年龄、临床类型及心源性猝死发生率的不同与基因突变有关(表2)。其中β-MHC基因突变是目前研究的热点,Anan将β-MHC错义突变分为3组:良性突变,外显子15,16,23上的保守性突变,估计寿命接近正常;恶性突变,外显子13,14,19上的突变,估计寿命明显缩短,早期病死率高,原因是基因突变阻抑了肌球蛋白的结构变化,或者是改变了肌球蛋白与肌动蛋白及其他分子间的相互作用;中性突变,多位于次要区域或在二级结构中产生中度变化,其表型介于良、恶性之间,可中度影响估计寿命。
HCM患儿心肌肥厚程度、肥厚的分布、发病年龄、临床类型及心源性猝死发生率的不同与基因突变有关(表2)。其中β-MHC基因突变是目前研究的热点,Anan将β-MHC错义突变分为3组:良性突变,外显子15,16,23上的保守性突变,估计寿命接近正常;恶性突变,外显子13,14,19上的突变,估计寿命明显缩短,早期病死率高,原因是基因突变阻抑了肌球蛋白的结构变化,或者是改变了肌球蛋白与肌动蛋白及其他分子间的相互作用;中性突变,多位于次要区域或在二级结构中产生中度变化,其表型介于良、恶性之间,可中度影响估计寿命。 另外,研究发现HCM患者中HLA-DRW4,A9,B5和B4抗原的检出率较高,梗阻性HCM患者中有HLA-DRW4者占73%。HCM与HLA-B27、DR3、DR4相关联。国内张之炯发现家族性HCM的致病基因或易感基因与HLA-DQA1与DQB1之间距离很近,认为HCM的致病除基因突变外,可能还存在1个位于HLA-DQA1与DQB1之间的易感基因。 (2)原癌基因表达异常:原癌基因(proto-oncogene)的活化与心肌肥厚的发生和发展密切相关。HCM患者心肌细胞内fos,myc和H-ras癌基因不同程度升高,去甲肾上腺素、血管紧张素Ⅱ和甲状腺素在心肌肥厚发生过程中起重要作用,与其促进原癌基因表达增强有关。去甲肾上腺素通过α受体激活磷酸肌醇/蛋白激酶-C系统而激活原癌基因。原癌基因参与心肌肥厚的形成,并可能是肥厚型心肌病的始动因素之一。 (3)儿茶酚胺异常:Grover-McKay等的研究表明,心脏内可能存在儿茶酚胺受体,服用致临界高血压剂量的去甲肾上腺素能引起HCM;刺激肾上腺素能神经可增加左室流出道的压力梯度并降低左室舒张顺应性,而β受体阻滞药可逆转上述反应;胎儿在发育期室间隔不成比例的增厚和心肌纤维排列紊乱之所以不能正常消退,可能是由于去甲肾上腺素和心肌受体之间存在缺陷而受阻所致,提示机体儿茶酚胺分泌增加和(或)机体对儿茶酚胺的过度敏感,可引起心脏功能和形态变化,导致HCM。 (4)钙调节异常:HCM仓鼠心肌细胞内钙增加,维拉帕米可起预防和治疗作用,实验性钙超载可引起心室舒张功能损害,用钙拮抗药可改善HCM的临床症状,高血钙常与HCM共存(47%~72%)。上述事实提示钙调节异常可能参与了HCM的发病,但有待于进一步证实。 (5)多因素作用:散发性病例可能是多因素作用的结果,具体机制不明。 2.继发性肥厚型心肌病 继发性HCM在婴儿多见,常见原因有: (1)小婴儿母亲患妊娠期糖尿病和胰岛细胞增殖症:妊娠期糖尿病使孕妇高血糖,造成胎儿也高血糖,从而刺激胎儿胰腺β细胞增生、肥大及胰岛素分泌增多;胰岛素的增多使胎儿机体内对胰岛素敏感的组织器官,如脂肪、肌肉、肝脏和心脏等体积可增加50%,而造成心肌肥厚。孕妇患胰岛细胞增殖症(nesidioblastosis)时,可直接造成孕妇高胰岛素血症,从而也使胎儿出现高胰岛素血症,同样可造成心肌肥厚。 (2)代谢缺陷病:如肉碱缺乏症、糖原贮积病、戈谢病、GM1和GM2神经节苷脂沉积病。代谢缺陷病是由于各种代谢酶的缺陷导致体内糖原、脂质等物质在心肌、肝脏等部位的沉积,在心肌组织中沉积而造成心肌肥厚。如糖原贮积病Ⅲ型(Pompe病)即是由于缺乏α-1,4-葡萄糖苷酶(酸性麦芽糖酶),引起糖原储积于肌肉和心脏,造成心肌肥厚。 (3)Noonan综合征:小儿HCM约1/3伴有此综合征,而此综合征中约25%有HCM,组织学上很难与家族性HCM区分。 (4)内分泌紊乱:垂体前叶过度分泌生长激素,可导致全身组织增生、肥大及物质代谢紊乱,使几乎所有的肢端肥大症患者心脏肥大,少数形成HCM。生长激素分泌过多引发HCM,与生长激素促进蛋白合成、使心肌细胞DNA合成增加、促进心肌肥大有关,同时全身脏器增大及高代谢亦使心脏负荷加重。动物实验表明,神经生长因子能引起心肌纤维排列紊乱及心肌肥厚;带有人的血管紧张素-Ⅰ受体(ATI-R)的基因模型[TGR(h-ANF-hAT1-R2)]研究表明,血管紧张素受体的输入可能是心肌肥厚的独立决定因素,同时发现钙的内环境改变亦可引起心肌肥厚,提示内分泌紊乱与HCM的发病有一定关系。内分泌紊乱引起的HCM与原发性HCM不同,其心室肌同轴性增厚,而非室间隔不对称性肥厚或乳头肌、心尖部局限性肥厚,同时有心腔扩大,而无左室流出道狭窄。 3.病理 (1)大体改变:外观心脏扩大,心
另外,研究发现HCM患者中HLA-DRW4,A9,B5和B4抗原的检出率较高,梗阻性HCM患者中有HLA-DRW4者占73%。HCM与HLA-B27、DR3、DR4相关联。国内张之炯发现家族性HCM的致病基因或易感基因与HLA-DQA1与DQB1之间距离很近,认为HCM的致病除基因突变外,可能还存在1个位于HLA-DQA1与DQB1之间的易感基因。 (2)原癌基因表达异常:原癌基因(proto-oncogene)的活化与心肌肥厚的发生和发展密切相关。HCM患者心肌细胞内fos,myc和H-ras癌基因不同程度升高,去甲肾上腺素、血管紧张素Ⅱ和甲状腺素在心肌肥厚发生过程中起重要作用,与其促进原癌基因表达增强有关。去甲肾上腺素通过α受体激活磷酸肌醇/蛋白激酶-C系统而激活原癌基因。原癌基因参与心肌肥厚的形成,并可能是肥厚型心肌病的始动因素之一。 (3)儿茶酚胺异常:Grover-McKay等的研究表明,心脏内可能存在儿茶酚胺受体,服用致临界高血压剂量的去甲肾上腺素能引起HCM;刺激肾上腺素能神经可增加左室流出道的压力梯度并降低左室舒张顺应性,而β受体阻滞药可逆转上述反应;胎儿在发育期室间隔不成比例的增厚和心肌纤维排列紊乱之所以不能正常消退,可能是由于去甲肾上腺素和心肌受体之间存在缺陷而受阻所致,提示机体儿茶酚胺分泌增加和(或)机体对儿茶酚胺的过度敏感,可引起心脏功能和形态变化,导致HCM。 (4)钙调节异常:HCM仓鼠心肌细胞内钙增加,维拉帕米可起预防和治疗作用,实验性钙超载可引起心室舒张功能损害,用钙拮抗药可改善HCM的临床症状,高血钙常与HCM共存(47%~72%)。上述事实提示钙调节异常可能参与了HCM的发病,但有待于进一步证实。 (5)多因素作用:散发性病例可能是多因素作用的结果,具体机制不明。 2.继发性肥厚型心肌病 继发性HCM在婴儿多见,常见原因有: (1)小婴儿母亲患妊娠期糖尿病和胰岛细胞增殖症:妊娠期糖尿病使孕妇高血糖,造成胎儿也高血糖,从而刺激胎儿胰腺β细胞增生、肥大及胰岛素分泌增多;胰岛素的增多使胎儿机体内对胰岛素敏感的组织器官,如脂肪、肌肉、肝脏和心脏等体积可增加50%,而造成心肌肥厚。孕妇患胰岛细胞增殖症(nesidioblastosis)时,可直接造成孕妇高胰岛素血症,从而也使胎儿出现高胰岛素血症,同样可造成心肌肥厚。 (2)代谢缺陷病:如肉碱缺乏症、糖原贮积病、戈谢病、GM1和GM2神经节苷脂沉积病。代谢缺陷病是由于各种代谢酶的缺陷导致体内糖原、脂质等物质在心肌、肝脏等部位的沉积,在心肌组织中沉积而造成心肌肥厚。如糖原贮积病Ⅲ型(Pompe病)即是由于缺乏α-1,4-葡萄糖苷酶(酸性麦芽糖酶),引起糖原储积于肌肉和心脏,造成心肌肥厚。 (3)Noonan综合征:小儿HCM约1/3伴有此综合征,而此综合征中约25%有HCM,组织学上很难与家族性HCM区分。 (4)内分泌紊乱:垂体前叶过度分泌生长激素,可导致全身组织增生、肥大及物质代谢紊乱,使几乎所有的肢端肥大症患者心脏肥大,少数形成HCM。生长激素分泌过多引发HCM,与生长激素促进蛋白合成、使心肌细胞DNA合成增加、促进心肌肥大有关,同时全身脏器增大及高代谢亦使心脏负荷加重。动物实验表明,神经生长因子能引起心肌纤维排列紊乱及心肌肥厚;带有人的血管紧张素-Ⅰ受体(ATI-R)的基因模型[TGR(h-ANF-hAT1-R2)]研究表明,血管紧张素受体的输入可能是心肌肥厚的独立决定因素,同时发现钙的内环境改变亦可引起心肌肥厚,提示内分泌紊乱与HCM的发病有一定关系。内分泌紊乱引起的HCM与原发性HCM不同,其心室肌同轴性增厚,而非室间隔不对称性肥厚或乳头肌、心尖部局限性肥厚,同时有心腔扩大,而无左室流出道狭窄。 3.病理 (1)大体改变:外观心脏扩大,心