概述
睫状环阻滞性青光眼(ciliary block glaucoma)是一种少见而严重的特殊类型闭角青光眼,它可造成一眼或双眼失明,准确的发病机制尚未清楚,对眼科医生来说本病仍然是个棘手的临床难题。von Graefe最早提出恶性青光眼(malignant glaucoma)的经典概念,即首先它被描述为直接继发于原发性闭角型青光眼手术后的一种特殊并发症,采用“恶性”一词是针对本病对传统青光眼治疗反应差和预后恶劣而言。其特点是中央前房极度变浅或消失,眼压升高,对传统的青光眼药物和手术治疗无效,疾病呈进行性或破坏性过程发展。随后提出过若干有关本病发病机制的假设及不同的命名术语,但恶性青光眼这一名称仍被...[详细]
病因
1.睫状体-晶状体或睫状体-玻璃体阻滞 许多研究曾发现恶性青光眼的患眼存在某些解剖结构异常,即在睫状突、晶状体和玻璃体前界膜三者之间(睫状环水平区域)的解剖关系异常。 经典的恶性青光眼几乎总是发生在具有眼前节解剖结构异常(如远视眼、小眼球和浅前房)的原发性闭角型青光眼术后,是否相对拥挤的眼前节(狭窄的眼前房和厚而前移的晶状体),同样亦存在相对狭窄的睫状环区。 睫状突、晶状体和玻璃体前界膜之间的解剖关系异常,也许是引起房水逆流和玻璃体腔内水囊形成的主要原因。一旦在手术、外伤、炎症或缩瞳剂等诱导下,这种解剖关系异常变得非常显著并表现为恶性循环过程。在强调睫状体或直接晶状体阻滞...[详细]
发病机制
对恶性青光眼目前尚缺乏公认的发病机制,下述乃几种比较流行的学说(图5,6,7)。 1.玻璃体内“水袋”形成学说 这一学说首先由Shaffer提出,以后为许多学者所接受,假设房水潴留在玻璃体后脱离之后,导致虹膜-晶状体或虹膜-玻璃体隔前移,引起前房普遍变浅,加重生理性瞳孔阻滞,甚至引起房角闭塞,导致眼压升高。借助超声波检查,可以证明玻璃体腔内水袋的存在。导致房水向后转移的机制尚不清楚,最大可能由于睫状体-晶状体阻滞所致。 2.睫状体-晶状体(或睫状体-玻璃体)阻滞学说 有人观察到恶性青光眼患者睫状突的顶端向前旋转压迫有晶状体眼的晶状体赤道部或无晶状体眼的前玻璃...[详细]
临床表现
恶性青光眼(睫状环阻滞性青光眼)综合征包含的临床类型分为传统性(经典)和非传统性(与恶性青光眼类似或相关)两大类。国内学者多主张分为原发性和继发性两大类,原发性者是指发生于具有眼球易感解剖结构异常的原发性闭角型青光眼患眼,可能包括:青光眼术后的经典恶性青光眼,经典恶性青光眼晶状体摘除术后的无晶状体性或人工晶状体性恶性青光眼,术前采用缩瞳剂或激光治疗引起的恶性青光眼。另有将其分为有晶状体、无晶状体或人工晶状体3种类型恶性青光眼,这种分类方法有利于认识玻璃体在恶性青光眼发病机制中的作用。考虑到目前国际上对青光眼分类有逐渐淡化原发性和继发性分类的倾向,也考虑到现代恶性青光眼的概念包括着一组与房水逆流...[详细]
并发症
前房严重炎症反应、脉络虹膜后粘连以及高眼压眼底损害等。
实验室检查
无特殊实验室检查。
其他辅助检查
主要采用超声及UBM检查。 1.经典恶性青光眼发作前的临床特点 (1)双眼具有眼前节狭小的解剖特点:中央前房深度常少于1.6mm或1.8mm;尤其双眼中央前房深度不对称,较浅眼的眼压亦较高和更易发生逆药性反应;晶状体较厚和位置相对前位(Lowe系数常低于0.18);眼轴较短。 (2)UBM检查发现:显示患眼的睫状体较厚、较前位(贴近周边虹膜),但也许正常,虹膜-晶状体隔前移,睫状突与晶状体赤道部的距离(睫状环)较小。 2.经典恶性青光眼发作时的早期特点 UBM检查发现虹膜-晶状体隔极度前移,虹膜从根部到瞳孔缘均与角膜内皮相贴,睫状突非常接近晶状体赤道部...[详细]
诊断
典型的(传统的)恶性青光眼的诊断可根据以下几点考虑:发生于急性或慢性闭角型青光眼的患者,行周边虹膜切除或小梁切除术后,眼压升高,前房普遍变浅或消失,有明显的晶状体虹膜隔前移,用缩瞳药治疗会使病情恶化,用散瞳睫状肌麻痹药可缓解病情加深前房,开放房角眼压下降。本病为双眼病,在同样诱因下,对侧眼也将发生恶性青光眼,对侧未发病眼滴缩瞳药后前房变浅,眼压升高即可确定诊断。
治疗
恶性青光眼一旦确诊,施行一般抗青光眼手术往往无效,并有招致病情恶化的危险;滴缩瞳药不能降压,反而引起眼压升高。局部滴散瞳睫状肌麻痹药,全身用高渗剂及碳酸酐酶抑制药是治疗本症的基础,局部及全身使用皮质类固醇是对本症有效的辅助治疗方法。 1.药物治疗 (1)散瞳睫状肌麻痹药:属于这类药物有阿托品、东莨菪碱、后马托品、乙酰环戊苯(Cyclopentolate)及托吡卡胺(Tropicamide)等。用这些药物的溶液滴眼,2~4次/d,可以使睫状肌松弛,睫状环阻滞缓解,晶状体韧带紧张,因而晶状体-虹膜隔向后移位,相对性瞳孔阻滞亦可缓解。前房恢复,眼压下降。对于有些晚期病例,药物疗效...[详细]
预后
及时有效控制恶性青光眼的发作,预后良好。
预防
手术后数小时需要进行裂隙灯显微镜检查,若发现前房极浅或消失和指测眼压升高,应立即开始标准恶性青光眼的综合药物治疗。恶性青光眼常发生在拆除或松解巩膜瓣缝线时,因此巩膜瓣缝线不宜拆除过快过多。同时术后睫状肌麻痹剂不宜过早停用。

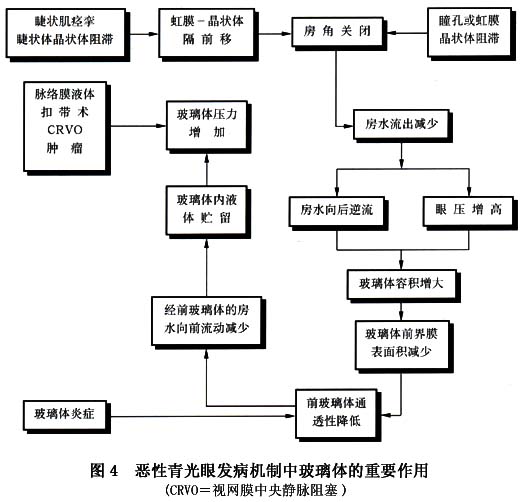
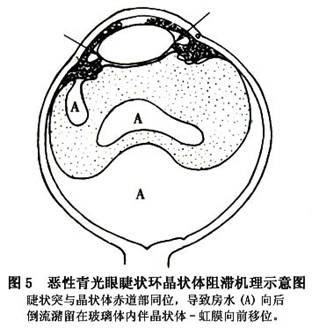
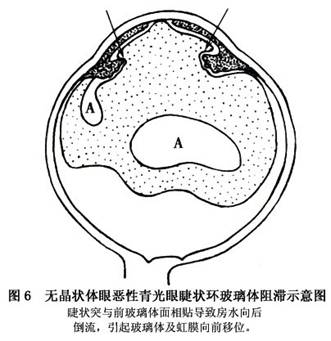
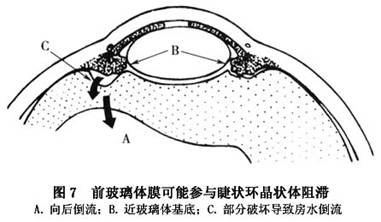 1.玻璃体内“水袋”形成学说 这一学说首先由Shaffer提出,以后为许多学者所接受,假设房水潴留在玻璃体后脱离之后,导致虹膜-晶状体或虹膜-玻璃体隔前移,引起前房普遍变浅,加重生理性瞳孔阻滞,甚至引起房角闭塞,导致眼压升高。借助超声波检查,可以证明玻璃体腔内水袋的存在。导致房水向后转移的机制尚不清楚,最大可能由于睫状体-晶状体阻滞所致。 2.睫状体-晶状体(或睫状体-玻璃体)阻滞学说 有人观察到恶性青光眼患者睫状突的顶端向前旋转压迫有晶状体眼的晶状体赤道部或无晶状体眼的前玻璃体膜,这就阻塞了房水向前流的通道,故主张将恶性青光眼称谓“睫状环阻滞性青光眼”以代替恶性青光眼。房水循环发生机械阻滞的原因可能与典型的恶性青光眼病人具有小眼球、小角膜、前房浅、晶状体厚以及视轴短等解剖因素有关,再加上滴缩瞳剂、外伤、手术及葡萄膜炎等诱因,可使睫状体水肿或痉挛,促使睫状体与晶状体(或玻璃体)进一步相贴近,从而导致眼压升高。 3.玻璃体及玻璃体前界膜阻滞学说 玻璃体前界膜可能参与恶性青光眼的形成,认为恶性青光眼者的玻璃体及玻璃体前界膜通透性降低,影响液体向前引流。灌注实验表明,当眼压升高时,通过玻璃体的液体流抗力也增加,因此导致经过玻璃体凝胶移动之液体减少。这种抗力增加可能由于玻璃体浓缩及其向前移位,因而前周边玻璃体与睫状体及晶状体赤道部处于同位相贴状态,减少了玻璃体前界膜可以通过液体的有效区域,进一步加重了玻璃体凝胶内液体向前移动的阻力。由于前后玻璃体的压力差,使浓缩的玻璃体凝胶向前移位,导致前房变浅。 4.晶状体韧带松弛学说 恶性青光眼者的晶状体-虹膜前移可能由于晶状体韧带松弛或软弱无力以及玻璃体的压力所致,另一些学者也提倡这一学说,而且认为晶状体韧带松弛系由于持续性房角闭塞的结果或者由于手术、缩瞳剂、炎症、外伤或其他不明原因引起的睫状肌痉挛的结果。由于晶状体韧带松弛,晶状体前后径增加,晶状体-虹膜隔前移,导致前房变浅。
1.玻璃体内“水袋”形成学说 这一学说首先由Shaffer提出,以后为许多学者所接受,假设房水潴留在玻璃体后脱离之后,导致虹膜-晶状体或虹膜-玻璃体隔前移,引起前房普遍变浅,加重生理性瞳孔阻滞,甚至引起房角闭塞,导致眼压升高。借助超声波检查,可以证明玻璃体腔内水袋的存在。导致房水向后转移的机制尚不清楚,最大可能由于睫状体-晶状体阻滞所致。 2.睫状体-晶状体(或睫状体-玻璃体)阻滞学说 有人观察到恶性青光眼患者睫状突的顶端向前旋转压迫有晶状体眼的晶状体赤道部或无晶状体眼的前玻璃体膜,这就阻塞了房水向前流的通道,故主张将恶性青光眼称谓“睫状环阻滞性青光眼”以代替恶性青光眼。房水循环发生机械阻滞的原因可能与典型的恶性青光眼病人具有小眼球、小角膜、前房浅、晶状体厚以及视轴短等解剖因素有关,再加上滴缩瞳剂、外伤、手术及葡萄膜炎等诱因,可使睫状体水肿或痉挛,促使睫状体与晶状体(或玻璃体)进一步相贴近,从而导致眼压升高。 3.玻璃体及玻璃体前界膜阻滞学说 玻璃体前界膜可能参与恶性青光眼的形成,认为恶性青光眼者的玻璃体及玻璃体前界膜通透性降低,影响液体向前引流。灌注实验表明,当眼压升高时,通过玻璃体的液体流抗力也增加,因此导致经过玻璃体凝胶移动之液体减少。这种抗力增加可能由于玻璃体浓缩及其向前移位,因而前周边玻璃体与睫状体及晶状体赤道部处于同位相贴状态,减少了玻璃体前界膜可以通过液体的有效区域,进一步加重了玻璃体凝胶内液体向前移动的阻力。由于前后玻璃体的压力差,使浓缩的玻璃体凝胶向前移位,导致前房变浅。 4.晶状体韧带松弛学说 恶性青光眼者的晶状体-虹膜前移可能由于晶状体韧带松弛或软弱无力以及玻璃体的压力所致,另一些学者也提倡这一学说,而且认为晶状体韧带松弛系由于持续性房角闭塞的结果或者由于手术、缩瞳剂、炎症、外伤或其他不明原因引起的睫状肌痉挛的结果。由于晶状体韧带松弛,晶状体前后径增加,晶状体-虹膜隔前移,导致前房变浅。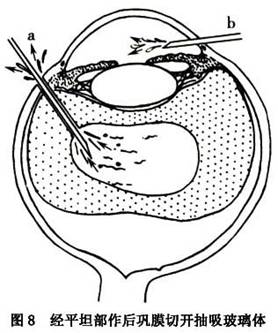 ①先在透明角膜缘作一板层斜面切开,为下一步前房注入空气做准备。 ②在颞下方切开球结膜,暴露巩膜,在角膜缘后3~5mm处作表面电烙,以角膜缘后3.5mm为中心作放射状巩膜切开,长2~3mm。 ③用止血钳在12mm处夹住18号针头,通过已散大之瞳孔,在检眼镜观察下,针头自颞下巩膜切口向视盘方向刺入12mm深,然后向前后移动针头,划破后玻璃体膜,让液体自动流出,或抽出1~1.5ml液体,眼球即变软。 ④通过预作的角膜缘切口,注射少量平衡盐液于前房,使眼球部分恢复球形。不必使眼球恢复正常压力,否则有引起眼压升高的危险。 ⑤局部即滴阿托品溶液,以后继续用此药物治疗。 (2)晶状体摘除术:当病人用最大限度药量仍不能降压,晶状体明显混浊或一眼已施晶状体摘除时,适于施行此手术,需同时切开玻璃体前界膜,多数病例可获得成功的治疗效果。 (3)后巩膜切开及前玻璃体切割术:细心进行玻璃体切割以除去部分前玻璃体,对治疗本症有一定疗效。但有潜在的严重并发症的可能,应慎重采用此治疗方法。 (4)激光治疗:通过虹膜切除区进行氩激光光凝睫状突,继而用药物治疗,已有报告可缓解恶性青光眼,推想这是由于破坏了睫状环-晶状体阻滞所致。一些发生在晶状体囊内摘除术后的恶性青光眼,这可能由于玻璃体前界膜通透力降低所致。有报告用YAG激光在玻璃体前界膜打孔可有满意疗效,勿需施行前玻璃体切割术。 (5)冷冻治疗:睫状体冷冻治疗恶性青光眼,推测其降压机制在于睫状体及玻璃体本身的改变。 3.对侧眼的处理 (1)一眼发生恶性青光眼,另一眼在相似的条件下,有很大机遇也要发生恶性青光眼,此已为许多学者所公认。若对侧眼眼压正常,房角开放,可试滴缩瞳剂数天,滴药后如果眼压升高,前房普遍变浅,表示此眼存在着易患恶性青光眼的因素,任何内眼手术均有诱发恶性青光眼发作的危险。 (2)如果对侧眼已处于闭角型青光眼早期,应尽早施周边虹膜切除术或激光虹膜切除术。如果已达发展期或晚期闭角型青光眼,施。
①先在透明角膜缘作一板层斜面切开,为下一步前房注入空气做准备。 ②在颞下方切开球结膜,暴露巩膜,在角膜缘后3~5mm处作表面电烙,以角膜缘后3.5mm为中心作放射状巩膜切开,长2~3mm。 ③用止血钳在12mm处夹住18号针头,通过已散大之瞳孔,在检眼镜观察下,针头自颞下巩膜切口向视盘方向刺入12mm深,然后向前后移动针头,划破后玻璃体膜,让液体自动流出,或抽出1~1.5ml液体,眼球即变软。 ④通过预作的角膜缘切口,注射少量平衡盐液于前房,使眼球部分恢复球形。不必使眼球恢复正常压力,否则有引起眼压升高的危险。 ⑤局部即滴阿托品溶液,以后继续用此药物治疗。 (2)晶状体摘除术:当病人用最大限度药量仍不能降压,晶状体明显混浊或一眼已施晶状体摘除时,适于施行此手术,需同时切开玻璃体前界膜,多数病例可获得成功的治疗效果。 (3)后巩膜切开及前玻璃体切割术:细心进行玻璃体切割以除去部分前玻璃体,对治疗本症有一定疗效。但有潜在的严重并发症的可能,应慎重采用此治疗方法。 (4)激光治疗:通过虹膜切除区进行氩激光光凝睫状突,继而用药物治疗,已有报告可缓解恶性青光眼,推想这是由于破坏了睫状环-晶状体阻滞所致。一些发生在晶状体囊内摘除术后的恶性青光眼,这可能由于玻璃体前界膜通透力降低所致。有报告用YAG激光在玻璃体前界膜打孔可有满意疗效,勿需施行前玻璃体切割术。 (5)冷冻治疗:睫状体冷冻治疗恶性青光眼,推测其降压机制在于睫状体及玻璃体本身的改变。 3.对侧眼的处理 (1)一眼发生恶性青光眼,另一眼在相似的条件下,有很大机遇也要发生恶性青光眼,此已为许多学者所公认。若对侧眼眼压正常,房角开放,可试滴缩瞳剂数天,滴药后如果眼压升高,前房普遍变浅,表示此眼存在着易患恶性青光眼的因素,任何内眼手术均有诱发恶性青光眼发作的危险。 (2)如果对侧眼已处于闭角型青光眼早期,应尽早施周边虹膜切除术或激光虹膜切除术。如果已达发展期或晚期闭角型青光眼,施。